Informaţii generale şi recomandări pentru efectuarea examenului coproparazitologic
Prin acest examen este detectată prezenţa unor paraziţi cu localizare intestinală, în limitele impuse de ciclul biologic al fiecărui parazit:
Protozoare: Giardia lamblia, Trichomonas intestinalis, Entamoeba spp., Blastocystis hominis
Helminţi
- Nematode:Ascaris lumbricoides, Trichuris trichiura, Enterobius vermicularis, Strongyloides stercoralis
- Trematode: Fasciola hepatica
- Cestode:Taenia spp., Hymenolepis nana, Diphyllobotrium latum1;3;6.
Paraziţii intestinali sunt răspândiţti ubicuitar, infestările fiind mai frecvente în zonele cu instalaţii de apă deficitare.
Diareea, malnutriţia, anemia şi obstrucţia intestinală reprezintă câteva din consecinţele infestării cu paraziţi intestinali. Protozoarele pot determina diaree şi/sau malabsorbţie atât prin secreţia de toxine, cât şi prin invadarea sau doar aderarea la mucoasa intestinală prin mecanisme necunoscute.
Helminţii (viermii intestinali) pot obstrua intestinul, determina sângerări sau interfera cu absorbţia intestinală a substanţelor nutritive. Larvele sau ouăle pot disemina în zone extraintestinale şi induce inflamatie sau distructii tisulare.
Unii paraziţi din categoría protozoarelor sau helmintilor pot habita tractul intestinal al omului şi animalelor fără a provoca manifestări clinice5.
Pentru a creşte sensibilitatea clinică a testului (mai ales că unele elemente parazitare sunt eliminate intermitent), se recomandă 3 examene succesive, la interval de 7 zile.
După tratarea unei parazitoze examenul coprologic de control se va efectua după un interval de timp variabil în funcţie de diagnostic. Astfel, după tratamentul unei infecţii cu protozoare, controlul se va efectua după 3-4 săptămâni iar in infecţiile cu helminţi după 1-2 săptămâni1;3;5;6.
Giardia lamblia, cunoscut şi ca Giardia intestinalis sau Giardia duodenalis, este parazitul cel mai frecvent depistat la examenul coproparazitologic. Reprezintă un organism unicelular (protozoar) prevăzut cu flageli care îi asigură mobilitatea. Este localizat în intestinul subţire (duoden şi jejun) unde se ataşează de microvilii enterocitelor prin intermediul unui disc adeziv. Datorită multiplicării sale extrem de rapide numărul elementelor parazitare poate depăşi 1 milion/cm. Consecinţele infestării sunt astfel tulburări de digestie şi absorbţie intestinală, cu spolierea treptată a organismului-gazdă de substanţele nutritive necesare. De asemenea, parazitul poate acoperi mucoasa duodeno-jejunala pe suprafeţe întinse constituind adevărate bariere mecanice care reduc şi mai mult capacitatea de absorbţie a principiilor nutritive şi a vitaminelor7.
Parazitul prezintă două forme de viaţă: trofozoit sau stadiul vegetativ şi chist sau stadiu de rezistenta. Are o înmulţire simplă prin diviziune binară. Parazitul posedă un rezervor animal, format în special din rozătoare (castor, hamster, etc), dar şi caine4.
Boala se transmite pe cale digestiva (fecal-orală) prin mâini murdare, consum de fructe şi/sau legume nespălate, precum şi de apa contaminată cu forma chistică a parazitului. Cel mai frecvent sunt afectaţi copiii mici din creşe şi grădiniţe, precum şi rudele acestora. Infecţia se transmite cu uşurinţă deoarece doza infectantă a chisturilor este redusă (~ 10 chisturi), chisturile sunt rezistente la clorinarea apei şi pot supravieţui câteva săptămâni în apa rece, precum şi din cauza existenţei rezervoarelor animale5.
După ingestie, procesul de dechistare are loc la nivelul duodenului şi în treimea proximală a duodenului şi jejunului sub acţiunea sucurilor digestive. Dechistarea este un proces rapid, terminându-se în 10 minute şi este semnalată de emergenţa flagelilor ventrali, ieşirea acestora fiind urmată de întreg trofozoitul. Trofozoitul se fixează de enterocit, se hrăneşte cu conţinutul intestinal şi, în decurs de 15-30 minute de la dechistare, începe să se dividă prin fisiune binară. Pe măsura ce parazitul antrenat de fluxul intestinal este împins în aval către colon, trofozoitul se autoprotejează de microambientul local prin conversie în forma chistică. Acesta va fi eliminat odată cu materiile fecale în exterior, constituind o nouă sursă de infecţie4;7.
Tabloul clinic include:
- infecţii silenţioase(mai ales la adulţi);
- giardioza acută: boală diareică acută combinată cu un sindrom gazos şi dispeptic biliar;
- giardioza cronică: disconfort digestiv persistent, episoade diareice alternând cu tranzit intestinal normal sau chiar încetinit.
Malabsorbţia de diverse grade este o complicaţie dezvoltată în aproximativ 10-15% dintre cazuri, atât în formele acute, cât şi cronice de boală. Alături de aceasta pot apărea alergodermii polimorfe complexe4.
Diagnosticul giardiozei se stabileşte cel mai frecvent prin examenul microscopic al materiilor fecale (depistarea chisturilor), precum şi prin testul imunoenzimatic (identicarea antigenul Giardia în scaun). Determinarea anticorpilor specifici nu prezintă utilitate datorită persistenţei îndelungate a acestora chiar şi în urma tratamentului eficace.
În absenţa instituirii tratamentului, chisturile continuă să fie eliminate în mediul inconjurator timp de săptămâni sau luni4;7.
Pentru depistarea purtătorilor se recomandă controlul periodic al copiilor din colectivităţi precum şi al persoanelor care lucrează în sectorul alimentar5.
Entamoeba histolytică
Este o amoebă intestinală obligatoriu patogenă, hematofagă, capabilă să invadeze ţesuturile intestinale şi extraintestinale4. Reprezintă agentul etiologic al amibiazei, boală cu evoluţie cronică ce este endemică în regiunile tropicale şi subtropicale umede, în special în India, Sri Lanka, Vietnam, Cambodgia, Indonezia, Malaezia.
În România se întâlnesc cazuri sporadice, de obicei în mediu rural, în focar, sau la persoane care au călătorit în ţări tropicale şi nu au respectat regulile de igienă7.
E. histolytica prezintă două forme morfologice:trofozoitsau stadiul vegetativ şi chist sau stadiul de rezistenţă. Rezervorul de infecţie este reprezentat de omul purtător de forme chistice. Transmiterea se face pe cale digestivă prin intermediul mâinilor murdare sau prin consumul de alimente contaminate cu ajutorul unor artropode (muşte, gândaci de bucătărie). Transmiterea hidrică este rară, dar are un potenţial epidemic4.
Parazitul se localizează la nivelul colonului, în special în colonul descendent şi sigmoid unde, datorită efectului său citolitic şi proteolitic asupra ţesuturilor, determină leziuni grave – abcese cu aspect de „buton de cămaşă”; în acest stadiu parazitul este hematofag. Tabloul clinic clasic este similar celui din dizenterie, cu scaune numeroase (15-20/zi), sărace cantitativ, însoţite de dureri abdominale şi tenesme rectale care sunt refractare la tratamentul cu antibiotice uzuale.
În absenţa tratamentului, trofozoiţii de E. histolytica se pot răspândi pe cale hematogenă la ficat, plămân sau creier, unde provoacă abcese amoebiene asociate cu un prognostic rezervat7.
Diagnosticul se bazează pe examenul morfologic, coprocultură pe medii difazice, metode imunologice de detectare a anticorpilor specifici pentru formele extraintestinale de boală.
Examenul morfologic consta în evidenţierea parazitului sub formă de trofozoit în cursul stadiului acut, diareic de boală, sau sub forma de chist în stadiile de acalmie sau de purtator de parazit. Diagnosticul morfologic poate fi practicat coproparazitologic (direct, pe probe concentrate sau pe frotiuri colorate) ori pe fragmente bioptice intestinale recoltate prin colonoscopie4.
Entamoeba coli
Este o amibă comensală care intră în alcătuirea florei intestinale normale, având rolul de a menţine un echilibru între diversele populaţii microbiene locale.
Nu are capacitate invazivă şi nici nu este hematofagă; prezintă ambele forme biologice de viaţă – trofozoit şi chist – cu o înmulţire prin diviziune binară. Devine patogenă numai în condiţiile alterării imunităţii locale, cel mai adesea după tratamente antibiotice prelungite. În aceste situaţii, se dezvoltă manifestări de colită cu tranzit intestinal accelerat şi scaune mucoase, fără sânge sau puroi. Deseori apar şi manifestări cutanate de hipersenasibilizare.
Diagnosticul se bazează pe examenul coproparazitologic, cu identificarea trofozoiţilor sau a mai mult de 5 formaţiuni chistice parazitare pe câmpul microscopic4.
Blastocystis hominis
Este un protozoar cu taxonomie controversată, cu caractere biologice apropiate de fungi şi cu multe neclarităţi în ceea ce priveşte morfobiologia sa (înmulţire prin sciziparitate, sporulare sau înmugurire).
Prezintă 4 forme morfologice majore:
- forma vacuolară – comensală, cel mai frecvent identificată, cu aspect de “rulment”;
- forma amoeboidală – identică cu cea vacuolară, cu excepţia formei neregulate datorată pseudopodelor; nucleii sunt poziţionaţi central iar vacuolele sunt absente;
- forma granulară – considerată forma oportunistă; prezintă 1-6 nuclei periferici iar citoplasma este ocupată de numeroase granule de dimensiuni variabile;
- forma chistică – controversata mult timp; existenţa sa este în prezent bine documentata, însă pentru a o identifica sunt necesare tehnici speciale de laborator.
Blastocystis hominis este un parazit cosmopolit, fiind întâlnit mai frecvent în regiuni cu deficienţe igienice; este comensal şi cu potenţial oportunist fiind implicat în infecţii severe la pacienţii imunodeprimaţi.
Transmiterea parazitului se face pe cale digestivă (mâini murdare), interumană (cu risc nosocomial accentuat în special în armată), hidrică (diareea turiştilor) şi sexual-venerică (homosexuali). Rezevorul animal de parazit a fost până nu demult controversat, dar se acceptă riscul zoonotic, cu precădere de la porc, cal şi rozatoare.
Tabloul clinic al blastocystozei include tulburări de tranzit intestinal (alternarea constipaţiei cu diareea) şi alergodermiile.
Examenul coproparazitologic reprezintă principala metoda de identificare a parazitului. Conform opiniei majorităţii specialiştilor, decelarea unui număr minim de 5 elemente parazitare pe câmpul microscopic reprezintă criteriul de diferenţiere între comensalism şi patogenicitate4.
Ascaris lumbricoides
Este un vierme cilindric (nematod) specific omului, cu dezvoltare obligatorie pe sol (geohelmint) şi răspândire ubicuitară. Prezintă dimorfism sexual, femela având dimensiuni de 25-31 cm şi masculul de 15-25 cm.
Ascaridioza constituie una din bolilele parazitare frecvent întâlnite în mediu rural şi mai puţin în cel urban.
Rezervorul de infecţie este reprezentat de omul parazitat cu Ascaris lumbricoides, femela fiind capabilă să depună zilnic în intestinul uman cca 200 000 ouă. Ajunse pe sol odată cu fecalele, ouăle neembrionate în momentul depunerii vor deveni embrionate după 5-7 zile de stagiu pe sol, la temperaturi de 20-24 ºC şi umidiate peste 10%. Omul se poate contamina cu ouă embrionate prin intermediul măinilor murdare şi prin ingerarea de legume/fructe nespălate. Insectele (muşte, gândaci) au un rol important în poluarea alimentelor cu ouă de Ascaris. După ce pătrund în intestinul omului sănătos (în special copii) ouăle îşi pierd invelişul protector şi pun în libertate embrionul (larva); acesta traversează activ peretele intestinal şi, prin intermediul circulatiei sangvine şi limfatice, ajunge în parenchimul hepatic, unde staţionează o perioadă de 4-5 zile. Ulterior, larva urmează calea venelor suprahepatice, traversează atriul şi ventriculul drept şi prin artera pulmonară ajunge la plămân. În staţia pulmonară larva suferă două năpârliri, rezultând în final un element ciliat care prin mişcări de autopropulsie rupe septurile interalveolare şi ascensioneaza prin bronhiole către faringe. În cavitatea orofaringiană larva poate urma două căi: fie va fi eliminată în exterior prin expectoraţie, fie va ajunge în intestin prin deglutiţie; în ultima situatie, larva are nevoie de 60-75 zile pentru a atinge stadiul de adult. Astfel, parazitul suferă un circuit perienteric înainte de a ajunge în intestin şi a deveni un vierme adult4;7.
Tabloul clinic reflectă etapele ciclului parazitar, existând manifestări provocate de larvele pulmonare şi de adulţii de la nivelul intestinului subţire:
– pneumonia interstiţială tranzitorie hipereozinofilică Loeffler: tuse spastică, wheezing, expectoraţie seroasă ce conţine eozinofile şi cristale Charcot-Leyden;
– alergii polimorfe;
– enterita ascaridiozică: dureri periombilicale, vărsături, tulburări de tranzit intestinal; numărul paraziţilor din intestin poate depăşi cifra de 40; la acest nivel exercită o acţiune mecanică, spoliatoare şi toxică putând genera obstrucţii intestinale şi malnutriţie protein-calorică.
Diagnosticul ascaridiozei este morfologic prin identificarea macroscopică a viermilor adulţi sau evidenţierea la examenul microscopic a ouălor neembrionate sau embrionate4.
Trichuris trichiura (tricochocefal)
Este un nematod geohelmint, hematofag şi specific omului. Adulţii trăiesc în cec şi colon prezentând dimensiuni medii: femela 3.5-5 cm lungime iar masculul 2-3.2 cm. Corpul este disproporţionat, primele 3/5 anterioare fiind subţiri şi efilate (cu rol în fixarea de mucoasa intestinală), iar cele 2- posterioare groase, plonjând în lumenul intestinal.
Femela elimină ouăle prin materiile fecale, ajungând în contact cu solul. Geombrionarea durează aproximativ 5-8 săptămâni. Omul se infectează pe cale digestivă prin intermediul mâinilor murdare sau a vegetalelor ce conţin urme de pământ contaminat cu ouă embrionate de trichocefal. Ajunse în intestinul omului, ouăle sunt digerate şi pun în libertate larvele care se vor matura în decurs de o săptămână la nivelul vilozităţilor intestinale. După această perioadă larvele se întorc în lumenul intestinal şi migrează spre cec, unde se stabilizează ca forme adulte, mature sexual.
Printre caracteristicile trichocefalului se numară capacitatea de a se insinua sub mucoasa intestinală prin intermediul capătului proximal, crearea unor denivelari cu zone microulcerate la locul de pătrundere şi hematofagia. Rezultă astfel o reacţie inflamatorie intestinală difuză, uneori cu aspect granulamatos, similar celui descris în boala Crohn.
Tabloul clinic este influenţat de încărcătura parazitară şi reactivitatea gazdei; se pot înregistra atât forme aşimptomatice asociate cu o încărcătură parazitară redusă, cât şi forme severe, asemănătoare bolilor inflamatorii intestinale (diaree sanguinolenta însotiţă de tenesme rectale şi dureri colicative, mai ales în fosa iliacă dreaptă). O complicaţie severă la copil o reprezintă prolapsul rectal. Hemoleucograma indică constant eozinofilie 10-15%.
Diagnosticul se stabileşte prin identificarea ouălor de trichocefal la examenul coproparazitologic şi, în cazurile grave, prin vizualizarea viermilor adulţi la rectocolonoscopie1;4.
Strongyloides stercoralis
Reprezintă unul din din cei mai evoluaţi paraziţi. Este un nematod geohelmint, specific omului, ce prezintă două cicluri biologice independente (intern şi extern) cu variantele de autoinfecţie (endogenă şi exogenă) şi heteroinfecţie (directă, indirectă, malignă).
În mod surprinzător, femela este vivipară eliminând direct prin orificiul uterin larve rabditoide, neinfecţioase, care ajung odată cu materiile fecale în exterior.
Ciclul direct de heteroinfecţie
În contact cu solul, larva rabditoidă se transformă prin năpârlire în larvă strongyloida infecţioasă care poate supravieţui în condiţii prielnice 2-3 săptămâni. Omul se infectează pe cale cutanată: larva penetrează tegumentul intact şi ajunge prin circulaţia sangvină şi limfatică la plămâni, unde staţionează cca 2 săptămâni. După ce suferă o nouă naparlire, larva rupe septurile interalveolare şi ascensionează prin bronhiole către faringe; din cavitatea orofaringiană ajunge prin deglutiţie în intestin unde va atinge stadiul de adult.
Ciclul indirect de heteroinfecţie
În condiţii neprielnice de mediu, larva rabditoidă ajunsă la sol se poate transforma direct în stadiul de adult liber. Aceşti paraziţi adulţi sunt capabili să se reproducă în sol, întreţinând astfel un rezervor teluric în aşteptarea condiţiilor favorabile dezvoltării larvelor infecţioase.
Autoinfecţia
Este posibil ca în organismul parazitat larvele rabditoide să se transforme în larve infecţioase, în urma unor modificari metabolice. Condiţiile care favorizează acest fenomen sunt constipaţia şi igiena precară. Autoinfectarea se poate produce în lumenul duodeno-jejunal, regiunea perianală şi epiteliul bronşic; stă la baza cronicizării bolii.
Hiperinfecţia sau ciclul malign
În condiţii de imunodepresie sistemică larva strongyloidă apare in situ la nivelul intestinului subţire. Acesta va traversa peretele intestinal şi va disemina pe calea circulaţiei limfatice şi sangvine în numeroase organe: ficat, plămâni, rinichi şi mai ales creier. Rata de mortalitate este ridicată.
Tabloul clinic include:
- manifestări cutanate: alergodermii;
- tulburări intestinale (enteropatia strongyloidozică): sindrom diareic cronic, grata persistenta, dureri colicative episodice;
- manifestări respiratorii: tuse cu expectoraţie seroasă, dispnee cu wheezing, dureri toracice;
- tulburări neuropsihice: anxietate, depresie;
- manifestări sistemice nespecifice: stare subfrebilă.
Hemograma indică eozinofilie 10-15%.
Diagnosticul strongyloidozei se bazează pe depistarea larvelor rabditoide în fecale, lichid duodenal, sputa sau lavaj bronholaveolar. În cazurile severe sunt necesare biopsii duodeno-jejunale4.
Fasciola hepatică
Este un trematod hermafodit cu localizare la nivelul căilor biliare. Este răspândit în zonele temperate, inclusiv România, rezervorul animal fiind reprezentat de ovine.
Adultul de Fasciola hepatică elimină oul neembrionat, neinfecţios prin bilă; oul traversează nemodificat tubul digestiv şi se excretă prin materiile fecale.
Pentru a-şi continua ciclul biologic, oul trebuie să ajungă în ape stătătoare calde unde embrionează şi, în decurs de 3 săptămâni, formează prima larvă – miracidium. Această forma larvară trebuie să întâlnească o gazdă intermediară – un melc din genul Lymnaea – în interiorul căreia se va genera în final larva infecţioasa denumită cercar. După ce părăseşte corpul melcului, cercarul înoată liber în apă, începe să secrete substanţe mucoide şi se înconjoară de un perete, devenind metacercar. Metacercarii sunt întâlniţi pe plantele acvatice, în mod particular în culturile de salată verde Cresson.
Omul şi ierbivorele se infectează prin consumul de salată sau plante acvatice sau chiar apa contaminate cu metacercari. Ajuns în intestinul uman, peretele metacercarului va fi digerat rapid iar larva rezultată va urma un traseu invaziv prin peretele intestinal, cavitatea peritoneală, capsula hepatică şi va atinge în final canaliculele biliare, în interiorul cărora se maturează în decurs de 3 luni. În traiectul său parazitul va provoca efecte mecanice de tip iritativ şi hemoragic, precum şi acţiuni toxice şi hipersensibilizante.
Tabloul clinic reflectă etapele de dezvoltare a parazitului şi include:
- faza migratorie sau acută: febră, stare generală alterată, prurit, dureri abdominale predominant în hipocondrul drept, diaree muco-sanguinolentă; eozinofilia este marcată (20-40%), iar testul hemoragiilor oculte în scaun este pozitiv că urmare a hemobiliei;
- faza obstructivă sau cronică: icter/subicter mecanic, asociat cu episoade colicative biliare;
- faza ectopică: forma aberantă de fascioloză ce cuprinde fascioloza cutanată şi fascioloza buco-faringiană (datorată consumului de ficat de miel, mai ales în regiunile din Orientul Mijlociu şi Africa de Nord).
Diagnosticul se bazează pe detectarea antigenelor sau anticorpilor specifici prin metode imunoenzimatice în faza acută şi cea obstructivă a bolii şi pe evidenţierea ouălor de Fasciola hepatică la examenul coproparazitologic sau în lichidul duodenal1;4.
Genul Taenia
Face parte din clasa cestodelor şi include două specii: Taenia saginata şi Taenia solium. Paraziţii se caracterizează printr-un corp aplatizat şi segmentat (în jur de 800-2000 segmente denumite proglote), de dimensiuni mari şi un cap (scolex) care prezintă organisme de fixare la peretele intestinal (ventuze şi/sau carlige). Pentru a fi asigurată dezvoltarea lor biologică, aceşti paraziţi au nevoie de o gazdă intermediară.
Rezervorul de infecţie este reprezentat de omul purtător de tenie în stadiul adult ale cărei proglote terminale, pline cu ouă (50 000-250 000/segment), se desprind în lumenul intestinal şi sunt eliminate activ în mediul exterior, prin fortarea sfincterului anal, independent de defecaţie. De aici, odată cu hrana, pot ajunge în intestinul unor animale care deţin rolul de gazdă intermediara şi care vor face forma larvară a infecţiei (cisticercoză).
Taenia saginata este un vierme plat cu dimensiuni mari (8-12 m), având un numar de 1000-2000 segmente, în timp ce Taenia solium are lungimi cuprinse între 2 şi 8 m şi prezintă 800-1000 segmente. Gazda intermediară este reprezentată de bovine în cazul Taeniei saginata şi de porcine în cazul Taeniei solium. Omul se infestează prin consumul de carne de vită/porc insuficient preparată termic, care conţine formele larvare (cysticercus bovis şi respectiv cysticercus cellulosae)7. În tubul digestiv al omului, corpul veziculos al larvei este digerat iar scolexul se evaginează şi se fixează de mucoasa intestinului cu ajutorul ventuzelor. După aproximativ 60-65 zile se va atinge stadiul adult, omul constituind astfel gazda definitivă pentru tenie4.
Tabloul clinic este dominat de eliminarea de proglote terminale; simptomatologia digestivă este similară celei din sindromul de colon iritabil: diaree mucoidă, uneori cu mulaje tubulare intestinale de mucus, însoţită de dureri abdominale cu carcater colicativ, greaţă, apetit modificat (bulimie sau, dimpotrivă, anorexie), scadere ponderală.
Diagnosticul se bazează fie pe examenul macroscopic al proglotelor eliminate, fie prin evidenţierea microcopică a ouălor de tenie4;7.
Hymenolepis nana
Este un vierme plat, segmentat (prezintă circa 200 segmente) cu o lungime de 2-4 cm, specific omului. Parazitul nu are nevoie de o altă gazdă în cursul dezvoltării sale biologice, astfel că omul reprezintă atât gazda definitivă, cât şi cea intermediară.
Rezervorul de infecţie îl constituie omul purtător de parazit, simptomatic sau nu, care elimină în mediul înconjurător odată cu materiile fecale ouăle embrionate. Omul sănătos se infectează pe cale digestivă prin intermediul mâinilor murdare sau consumul de vegetale contaminate cu ouă embrionate de Hymenolepis nana. De asemenea, există posibilitatea unei autoinfecţii endogene, datorită numărului foarte mare de paraziţi (zeci-sute) care populează intestinul la un moment dat.
În intestinul omului se dezvoltă atât formele larvare (cisticercoizi), cat şi formele adulte; ciclul se numeşte autoxen şi are o durată totală de 21-30 zile7.
Infecţiile mici şi medii cu Hymenolepis nana pot evolua asimptomatic; în cursul infecţiilor masive se întâlneşte tabloul clinic de abdomen cronic dureros: colici abdominale, tranzit intestinal alternant, tulburări de apetit, scădere ponderală, tulburări neuropsihice nespecifice.
Diagnosticul se bazează în principal pe identificarea ouălor caracteristice la examenul coproparazitologic4;7.
Dyphilobothrium latum (botriocefal)
Este o cestodă cu corpul plat format din 2000-4000 segmente (proglote) şi cu o lungime de 10-16 m. Se fixează în intestinul omului cu ajutorul a două ventuze, situate la nivelul scolexului ce are o formă ovoidal-migdalată caracteristică.
Parazitul are nevoie în cursul dezvoltarii sale biologice de două gazde intermediare (un crustaceu din genul Cyclops şi peşti răpitori: ştiuca, biban, crap, mihalt) în organismul cărora se vor dezvolta larvele. Omul sănătos se infectează pe cale digestivă prin consumul de peşte crud şi icre ce conţin larve închistate7. În intestinul omului scolexul evaginează şi se fixează cu ventuzele de mucoasă; stadiul de adult este atins după 70-90 zile, omul constituind astfel gazda definitivă pentru parazit. Viermele adult elimină un număr mare de ouă (până la un milion/zi) care vor fi excretate în mediul înconjurător odată cu materiile fecale.
Botriocefalul nu distruge enterocitul şi, în consecinţă, nu provoacă un sindrom de malabsorbţie. În schimb, exercită o acţiune de spoliere selectivă prin consumul de vitamina B12 şi acid folic; de asemenea, prin poziţionarea sa în jejunul superior poate bloca receptorii pentru factorul intrinsec. Din aceste motive se întâlneşte frecvent în botriocefaloza anemia megaloblastică. Alături de posibilitatea expulzarii spontane a viermelui în cursul defecţiei, persoanele afectate mai pot prezenta o simptomatologie digestivă similară teniazei.
Diagnosticul se bazează în principal pe identificarea ouălor de botriocefal la examenul coproparazitologic4.
Pregătire pacient
Pacientul va evita:
– înainte de recoltare: examenul radiologic gastrointestinal baritat, administrarea de laxative;
– in săptămâna premergătoare recoltării, administrarea anumitor medicamente: bismut, Metamucil, uleiuri minerale, Tetraciclina, antiamoebiene, antidiareice, antiacide2;8.
Specimen recoltat – materii fecale din orice moment al zilei; se recoltează câte o porţiune de mărimea unei alune, din 3 locuri diferite ale bolului fecal2.
Cauze de respingere a probei
– specimen obţinut cu uleiuri minerale, bismut, compuşi de magneziu;
– recipient murdar pe exterior;
– specimen contaminat cu urină2;8.
Recipient de recoltare – recipient de unică folosinţă pentru fecale bine închis cu capac; este interzisă adăugarea de substanţe conservante2;8.
Stabilitate probă – examinarea promptă a scaunului este importantă pentru scaunele lichide sau moi care ar putea conţine trofozoiţi de protozoare; scaunele formate, care pot conţine chişti de protozoare, ouă sau larve de helminţi pot rămâne câteva ore la temperatura camerei sau până a doua zi la frigider6.
Prelucrare necesară după recoltare – analiza se execută din materii fecale proaspăt emise (de preferat); dacă acest lucru nu este posibil, proba va fi păstrată la 2-8ºC 2;8.
Metodă – examen macroscopic + examen microscopic direct (intre lama şi lamela)2;8.
Valori de referinţă – absente elemente parazitare intestinale2.
Interpretarea rezultatelor
Examenul macroscopic
Examinarea se face direct în recipientul în care s-a prelevat proba, cu ohiul liber sau cu lupa de mână, utilizând o baghetă de sticlă sau o ansă. Se observă culoarea, mirosul, consistenţa scaunului, prezenţa de mucus, puroi, sânge, precum şi de elemente suspecte ca fiind parazitare. Dintre elementele parazitare se pot observa:
– proglote de Taenia spp.
Proglotele de Taenia saginată (rar vizibile în materiile fecale, deoarece se elimină prin orificiul anal între defecaţii) sunt dreptunghiulare de 2 cm lungime/0,5 cm lăţime, au uterul bine dezvoltat, prevăzut cu 20-30 de ramificaţii închise în deget de mănuşă, pline cu ouă şi au mişcari periodice caracteristice. Proglotele de Taenia solium au dimensiuni de 2 cm lungime/6-8mm lăţime, uterul lor prezintă 7-10 ramificaţii laterale, închise în deget de mănuşă pline de ouă) fără a prezenta mişcări.
– viermi adulţi de Ascaris lumbricoides.
Au corpul cilindric, de culoare roz-albicioasă şi prezintă striuri discrete longitudianle. Se va preciza sexul viermelui eliminat. Femelele au 20-30 cm lungime/5-6 mm grosime. Masculii sunt mai mici, au 15-20 cm lungime şi extremitatea posterioară incurbată.
Examenul microscopic direct
Se examinează între lamă şi lamelă o cantitate mică de materii fecale (1.5 – 2 mg), prelevată din diferite părţi ale probei, amestecată în ser fiziologic sau soluţie Lugol.
Pentru realizarea preparatelor se folosesc lame curate, degresate. Pe o lamă se pune o picătura de ser sau soluţie Lugol. Cu ajutorul unei baghete se prelevă o mică cantitate din proba de examinat şi se amestecă pe lamă cu picătura de ser sau soluţie Lugol. Se acoperă cu o lamelă.
Preparatul trebuie examinat cât mai repede pentru a se evita uscarea. Se utilizează lamele de 18/18 mm dimensiuni, astfel încât marginile lor să fie cuprinse în interiorul marginilor lamei. Suspensia trebuie să fie uniformă, iar lamela aşezată orizontal, nu înclinat.
Preparatul se examinează în întregime, deplasând lama de la stânga la dreapta şi de sus în jos.
Examinarea se face cu obiectiv 10x sau 20x, iar identificarea fiecărui element parazitar decelat se face cu obiectivul 40x; se utilizează oculare 10x.
La examinarea microscopică se pot depista diferite specii de paraziţi.
Giardia lamblia. Poate apărea sub două forme: trofozoit (forma vegetativă) şi chist. Forma vegetativă se întâlneşte excepţional, doar în scaunele apoase, în stadiul acut al bolii, mai ales la copii (în 5-10% din cazuri). Trofozoitul este piriform de 15 µm lungime/6-10 µm lăţime. Are corp cu simetrie bilaterală cu 2 nuclei, 4 perechi de blefaroplasti şi 4 perechi de flageli, un disc adeziv şi un axostil.
Fig. 21.4.8.1 Trofozoiţi de Giardia lamblia (după MicrobeLibrary.com)
Chistul este ovalar şi are 9-13 µm lungime / 6µm lăţime. Are o membrană externă fină, dublă, 4 nuclei şi un mănunchi de flageli. Nucleii au o dispoziţie variabilă, frecvent sunt grupaţi la o extremitate a celulei.
În axul chistului se observă resturi flagelare cu dispoziţie sinuoasă, în formă de S.
Fig. 21.4.8.2 Chisturi de Giardia lamblia (preparat în soluţie salină – imagine din colecţia proprie a laboratorului)
În preparatul nativ efectuat în soluţie Lugol chisturile sunt evidente, fiind colorate în brun.
Cu obiectivul de 40 x se detectează detalii structurale şi aspecte diferite:
a) chisturi mari, oval rotunde, colorate brun deschis; sunt chisturi tinere, recent formate, bine hidratate; dubla membrană se observă net, dar nucleii şi mănunchii de flageli sunt mai estompaţi;
b) chisturi de dimensiuni medii, ovale, colorate brun închis; dublul contur se distinge mai greu, dar interiorul chistului este net.
c) chisturi mici albastre sau palid cenuşii; sunt rar observate (2-3%); nu au contur dublu şi au interior omogen; sunt chisturi neviabile.
Fig. 21.4.8.3 Chist de Giardia lamblia (preparat nativ în soluţie Lugol – imagine de la www.dpd.cdc.gov)
Entamoeba histolytica. Chistul matur este rotund, cu dimensiuni de 10-20 µm şi cu un număr constant de 4 nuclei; conţinutul chistului este relativ compact, fiind întâlnite 1-4 baghete cu capete rotunjite, denumite corpi siderofili sau cromatoizi.
Fig. 21.4.8.4 Chist de Entamoeba histolytica (preparat nativ – imagine de la www.dpd.cdc.gov)
Entamoeba coli. Chistul matur are dimensiuni variabile (10-30 µm), cu un perete gros, dublu-lamelar şi un conţinut granular uniform ce îi conferă în preparatele proaspete o coloraţie gri-cenuşie; numărul nucleilor este constant de 8, asezaţi în acelaşi plan sau în planuri diferite.
Fig. 21.4.8.5 Chist de Entamoeba coli (preparat nativ – imagine de la www.dpd.cdc.gov)
Blastocystis hominis. Forma vacuolară (considerată de unii drept chist) este sferică sau elipsoidală şi are în medie 8-10 µm. Poate prezenta o capsulă proeminentă; conţine o vacuolă mare centrală, clară, delimitată de o bandă subţire neregulată din citoplasma, la nivelul căreia se găsesc nucleii şi granulele dispuse periferic.
Deţine în general un nucleu, dar uneori poate avea 2-4 nuclei sau chiar mai mulţi. La formele binucleate, nucleii pot fi dispuşi la cei doi poli, iar la formele tetranucleate la periferia celule.
Fig.21.4.8.6 Blastocystis hominis – forma vacuolara (preparat nativ în soluţie salină – imagine de la www.dpd.cdc.gov)
Ascaris lumbricoides. Oul este oval, de 65-80 µm/ 50 µm. Prezintă un înveliş dublu: un înveliş extern, gros, cu aspect mamelonat caracteristic şi un înveliş intern de natură chitinoasa, neted, transparent, stratificat.
Oul neembrionat prezintă în interior celula-ou, înconjurată de masa vitelină, retractată, lăsând un spaţiu liber între ea şi învelişurile externe. Forma şi dimensiunile oului embrionat sunt asemănătoare cu ale celui neembrionat, dar in interiorul lui se dezvoltă o larvă cilindrică de 250 µm, răsucită în jurul său, în forma literei S, ocupând în întregime interiorul oului.
Fig. 21.4.8.7 Ou de Ascaris lumbricoides (preparat nativ în soluţie salină – imagine din colecţia proprie a laboratorului)
Trichiuris trichiura (Tricocefalul). Oul este oval, brun, de 50 / 22 µm. Prezintă un înveliş extern gros şi, în interior, celula-ou înconjurată de masa vitelină. La cei doi poli există dopuri albuminoase transparente, care conferă oului un aspect caracteristic de lămâie.
Fig. 21.4.8.8 Ou de Trichuris trichiura (preparat nativ în soluţie salină – imagine din colecţia proprie a laboratorului)
Strongyloides stercoralis. Deoarece ouăle eclozează imediat după emisie şi eliberează larve în lumenul intestinal, în materiile fecale se vor evidenţia doar larve.
Larvele rabditoide măsoară 250-300 µm, au un esofag “bicameral” (o porţiune proximală cilindrică de calibru redus şi un segment distal globulos “în bulb de ceapă”) şi o extremitate posterioară ascuţită.
Fig. 21.4.8.9 Larva rabditoida de Strongiloides (preparat nativ în soluţie salină – imagine din colecţia proprie a laboratorului)
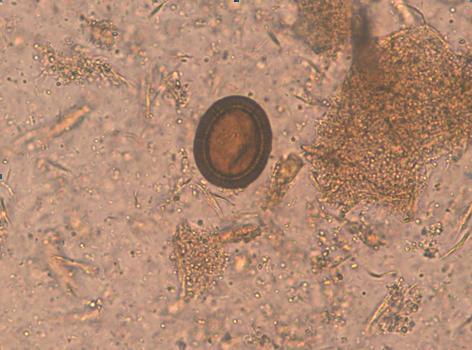
Fasciola hepatică. Ouăle sunt neembrionate, cu dimensiuni de 140/ 80 µm, culoare galben brună, prezentând la exterior o coajă subţire, deformabilă, cu un opercul la un pol, iar în interior celula ou inconjurată de masa vitelină.
Fig. 21.4.8.10 Ou de Fasciola hepatica (preparat nativ în soluţie salină – imagine de la www.dpd.cdc.gov)
Taenia solium şi Taenia saginata. Ouăle sunt embrionate, rotund-ovalare, având dimensiuni de 30-50 µm. Prezintă o coroană periferică striată caracteristică, alcătuită din trei membrane embrionare; conţin în interior o substanţă vitelină galben-maronie şi un embrion hexacant, cu 6 carlige dispuse în perechi.
Fig. 21.4.8.11 Ou de Taenia spp. (preparat nativ în soluţie salină – imagine din colecţia proprie a laboratorului)
Hymenolepis nana. Ouăle sunt transparente, având dimensiuni de 47/37 µm. Prezintă un embrion hexacant (cu trei perechi de cârlige) şi un înveliş dublu alcătuit dintr-o membrană externă fragilă şi o membrană internă densă, cu două proeminente care-i conferă aspect de lămâie şi de la nivelul cărora pornesc 4-8 filamente dispuse între cele două membrane ale oului.
Fig.21.4.8.12 Ou de Hymenolepis nana (preparat nativ în soluţie salină – imagine de la www.dpd.cdc.gov)
Diphylobothrium latum. Ouăle sunt neembrionate, au aspect oval, culoare brună şi dimensiuni de 70/45 µm. Prezintă un înveliş extern dedublat, cu un opercul la unul din poli şi o mică proeminenţă (carenă) la polul opus; în interior se găseşte celula-ou înconjurată de masa vitelină1;2 ;4 ;6.
Fig.21.4.8.13 Ouă de Diphylobothrium latum (preparat nativ în soluţie Lugol – imagine de la www.dpd.cdc.gov)
Limite şi interferenţe
Un rezultat pozitiv indică prezenţa parazitului, dar aceasta nu implică întotdeauna că parazitul este responsabil pentru simptomele pacientului5.
Un singur examen negativ nu exclude posibilitatea infestării parazitare.
Examenul pentru Giardia poate fi negativ în stadiile precoce ale infestării, în infestări cronice şi la pacienţii care elimină ciclic parazitul.
Rezultate fals negative pot să apară dacă în săptămâna care precede testul s-au administrat bariu, bismut, Metamucil, uleiuri minerale, Tetraciclina, medicamente antiamoebiene, antidiareice, antiacide.
În toate aceste cazuri se recomandă determinarea de antigen Giardia în fecale1;3..
Acest test nu este indicat pentru depistarea Toxoplasmei gondii, Toxocarei canis, Plasmodium spp sau Trichomonas deoarece aceste organisme nu apar în materiile fecale.
Ouăle de Enterobius vermicularis sunt rar întâlnite în materiile fecale (doar în infestările masive) datorită particularităţilor ciclului evolutiv. Atunci când există suspiciunea clinică, se indică efectuarea amprentei anale.
Pentru identificarea ouăchistilor sporozoarelor digestive (Cryptosporidium parvum şi Cyclospora cayetanensis) este necesară efectuarea de froturi colorate cu coloraţii speciale (Ziehl-Neelsen modificata Hendricksen-Pohlentz)4.
Bibliografie
1. Dan Steriu. Infecţii parazitare, Editura Ilex, Bucuresti 2003, 26-34, 152-155, 161-166, 221-226, 231-234, 243-246, 247-250.
2. Laborator Synevo. Referinţele specifice tehnologiei de lucru utilizate 2006. Ref Type: Catalog.
3. Laboratory Corporation of America. Directory of Services and Interpretive Guide. Giardia lamblia by EIA and Ova and Paraşites Examination. www.labcorp.com. 2003. Ref Type: Internet Communication.
4. Lidia Lazar. Compendiu de parazitologie medicală – Paraziţii în Patologia Umană. Editura Universitară “Carol Davila”, Bucureşti, 2006.
5. Mayo Clinic/Mayo Medical LaboratoriesTest Catalogs and Guides. Paraşitic Examination. www.mayomedicallaboratories.com. Ref Type: Internet Communication.
6. Simona Rădulescu, Meyer Ernest. Diagnosticul bolilor parazitare. În Parazitologie medicală, Editura All, Bucureşti,1992, 271-275.
7. Valeriu Ştefănoiu. Diagnosticul infecţiilor parazitare. Prezentare Congres SRML 2010.
8. World Health Organisation Geneva Basic Laboratory Methods in Medical Parasitology, 1991.